Перманганат калия
| Перманганат калия | |
|---|---|
 | |
 | |
| Общие | |
| Систематическое наименование |
Перманганат калия |
| Традиционные названия | Марганцовокислый калий, марганцовка |
| Хим. формула | KMnO4 |
| Физические свойства | |
| Состояние | твердое (хрупкие кристаллы) |
| Молярная масса | 158,034 г/моль |
| Плотность | 2,703 г/см³ |
| Термические свойства | |
| Температура | |
| • разложения | 240 °C |
| Мол. теплоёмк. | 119,2 Дж/(моль·К) |
| Энтальпия | |
| • образования | −813,4 кДж/моль |
| Химические свойства | |
| Растворимость | |
| • в воде | 6,38 (20 °C) |
| Классификация | |
| Рег. номер CAS | 7722-64-7 |
| PubChem | 516875 |
| Рег. номер EINECS | 231-760-3 |
| SMILES | |
| InChI | |
| RTECS | SD6475000 |
| Номер ООН | 1490 |
| ChemSpider | 22810 |
| Безопасность | |
| Пиктограммы СГС |
|
| NFPA 704 | |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |


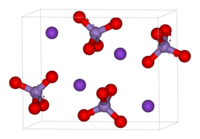
Пермангана́т ка́лия (лат. Kalii permanganas, распространённое название в быту — марганцо́вка) — марганцовокислый калий, калиевая соль марганцовой кислоты. Химическая формула — KMnO4. Представляет собой тёмно-фиолетовые, почти чёрные кристаллы, при растворении в воде образующие ярко окрашенный раствор цвета фуксии.
Физические свойства
[править | править код]Внешний вид: тёмно-фиолетовые кристаллы с металлическим блеском. Показатель преломления составляет 1,59 (при 20 °C).
Растворяется в воде (см. таблицу), жидком аммиаке, ацетоне (2:100), метаноле, пиридине.
| Температура, °C | 10 | 20 | 25 | 30 | 40 | 50 | 65 |
|---|---|---|---|---|---|---|---|
| Растворимость, г/100 г воды | 4,22 | 6,36 | 7,63 | 9 | 12,5 | 16,8 | 25 |
Термодинамические свойства
[править | править код]| Стандартная энтальпия образования ΔH | −813,4 кДж/моль (т) (при 298 К) |
|---|---|
| Стандартная энергия Гиббса образования G | −713,8 кДж/моль (т) (при 298 К) |
| Стандартная энтропия S | 171,71 Дж/(моль·K) (т) (при 298 К) |
| Стандартная мольная теплоёмкость Cp | 119,2 Дж/(моль·K) (т) (при 298 К) |
Химические свойства
[править | править код]| Окисленная форма | Восстановленная форма | Среда | E0, В |
|---|---|---|---|
| MnO4− | MnO42− | OH− | +0,56 |
| MnO4− | H2MnO4 | H+ | +1,22 |
| MnO4− | MnO2 | H+ | +1,69 |
| MnO4− | MnO2 | OH− | +0,60 |
| MnO4− | Mn2+ | H+ | +1,51 |


Является сильным окислителем. В зависимости от pH раствора окисляет различные вещества, восстанавливаясь до соединений марганца разной степени окисления. В кислой среде — до соединений марганца(II), в нейтральной — до соединений марганца(IV), в сильно щелочной — до соединений марганца(VI). Примеры реакций приведены ниже (на примере взаимодействия с сульфитом калия):
- в кислой среде:
- ;
- в нейтральной среде:
- ;
- в щелочной среде:
- .
Однако последняя реакция (в щелочной среде) идёт по указанной схеме только при недостатке восстановителя и высокой концентрации щёлочи, которая обеспечивает замедление гидролиза манганата калия.
При соприкосновении с концентрированной серной кислотой перманганат калия взрывается, однако при аккуратном соединении с холодной кислотой реагирует с образованием неустойчивого оксида марганца(VII):
- .
При этом в качестве промежуточного продукта может образовываться интересное соединение — оксосульфат марганца . По реакции с фторидом иода(V) можно получить аналогичный оксофторид:
- .
При нагревании разлагается с выделением кислорода (этим способом пользуются в лаборатории для получения чистого кислорода). Схему реакции упрощённо можно представить уравнением:
- .
На самом деле реакция идёт намного сложнее, например, при не очень сильном нагревании её можно примерно описать уравнением:
- .
Реагирует с солями двухвалентного марганца, например:
- .
Эта реакция в принципе обратна дисмутации (диспропорционирование) : : на и .
Окисляет органические вещества. В частности, разбавленные растворы перманганата калия в щелочной и нейтральной среде окисляют алкены до диолов (реакция Вагнера):
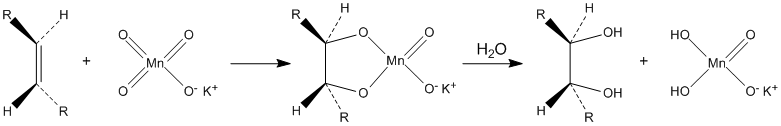 Водные растворы перманганата калия термодинамически нестабильны, но кинетически довольно устойчивы. Их сохранность резко повышается при хранении в темноте.
Водные растворы перманганата калия термодинамически нестабильны, но кинетически довольно устойчивы. Их сохранность резко повышается при хранении в темноте.
При смеси с пероксидом водорода протекает следующая реакция:
- .
Перманганат калия реагирует с концентрированной соляной, бромоводородной или иодоводородной кислотой. В результате выделяются свободные галогены:
Во время химической реакции хлорид-анион окисляется до элементарного хлора, а ион в перманганат-анионе восстанавливается до катиона :
Применение
[править | править код]Применение этой соли чаще всего основано на высокой окисляющей способности перманганат-иона, обеспечивающей антисептическое действие.
Медицинское применение
[править | править код]| Перманганат калия | |
|---|---|
| Kalii permanganas | |
| Химическое соединение | |
| ИЮПАК | Перманганат калия |
| Брутто-формула | KMnO4 |
| CAS | 7722-64-7 |
| PubChem | 516875 |
| DrugBank | DB13831 |
| Состав | |
| Классификация | |
| Фармакол. группа | Антисептики и дезинфицирующие средства |
| АТХ | D08AX06 |
| Лекарственные формы | |
| порошок для приготовления раствора | |
| Другие названия | |
| KMnO4, Калия перманганат, Марганцовка, Хамелеон минеральный, Марганцевокислый калий, Марганцовокислый калий, Калий марганцевокислый | |
Разбавленные растворы (около 0,1 %) перманганата калия нашли широчайшее применение в медицине как антисептическое средство, для полоскания горла, промывания ран, обработки ожогов. В качестве рвотного средства для приёма внутрь при отравлениях морфином, аконитином и некоторыми другими алкалоидами используют разбавленный (0,02—0,1 %) раствор перманганата калия[1].
Фармакологическое действие
[править | править код]Антисептическое средство. При соприкосновении с органическими веществами выделяет атомарный кислород. Образующийся при восстановлении препарата оксид образует с белками комплексные соединения — альбуминаты (за счёт этого калия перманганат в малых концентрациях оказывает вяжущее, а в концентрированных растворах — раздражающее, прижигающее и дубящее действие). Обладает также дезодорирующим эффектом. Эффективен при лечении ожогов и язв. Способность калия перманганата обезвреживать некоторые яды лежит в основе использования его растворов для промывания желудка при отравлениях неизвестным ядом и пищевых токсикоинфекциях. При попадании внутрь всасывается, оказывая действие (приводит к развитию метгемоглобинемии).
Показания
[править | править код]Смазывание язвенных и ожоговых поверхностей — инфицированные раны, язвы и ожоги кожи. Полоскание полости рта и ротоглотки — при инфекционно-воспалительных заболеваниях слизистой оболочки полости рта и ротоглотки (в том числе при ангинах). Для промывания и спринцеваний при гинекологических и урологических заболеваниях — кольпиты и уретриты. Для промываний — желудка при отравлениях, вызванных приёмом внутрь алкалоидов (морфин, аконитин, никотин), синильной кислотой, фосфором, хинином; кожи — при попадании на неё анилина; глаз — при поражении их ядовитыми насекомыми.
Противопоказания
[править | править код]Гиперчувствительность.
При передозировке: резкая боль в полости рта, по ходу пищевода, в животе, рвота, диарея; слизистая оболочка полости рта и глотки — отёчная, тёмно-коричневого, фиолетового цвета, возможен отёк гортани, развитие механической асфиксии, ожогового шока, двигательного возбуждения, судорог, явлений паркинсонизма, геморрагического колита, нефропатии, гепатопатии. При пониженной кислотности желудочного сока возможно развитие метгемоглобинемии с выраженным цианозом и одышкой. Смертельная доза для детей — около 3 г, для взрослых — 0,3—0,5 г/кг.
Лечение: метиленовый синий (50 мл 1 % раствора), аскорбиновая кислота (внутривенно — 30 мл 5 % раствора), цианокобаламин — до 1 мг, пиридоксин (внутримышечно — 3 мл 5 % раствора).
Способ применения и дозы
[править | править код]В водных растворах для промывания ран (0,1—0,5 %), для полоскания рта и горла (0,01—0,1 %), для смазывания язвенных и ожоговых поверхностей (2—5 %), для спринцевания (0,02—0,1 %) в гинекологической и урологической практике, а также промывания желудка при отравлениях.
Предосторожности
[править | править код]Активно взаимодействует при нагреве и даже при комнатной температуре с большинством восстановителей, например, органическими веществами (сахарозой, танинами, глицерином и многими другими), легкоокисляющимися веществами, поэтому при смешивании происходит саморазогревание, что иногда вызывает самовоспламенение смеси (с концентрированным раствором глицерина, или безводным — всегда) и может привести к взрыву.
Очень опасно растирание сухого перманганата калия с органическими веществами и порошками активных металлов и неметаллов (кальцием, алюминием, магнием, фосфором, серой и др.) — весьма вероятен взрыв.
Применение в аналитической химии
[править | править код]Благодаря сильным окислительным способностям перманганат-иона в кислое среде и его крайне яркой окраске, он часто используется в качестве титранта, которому не требуется индикатор (конец титрования определяется по неисчезающей розоватой окраске). Для стандартизации раствора, в качестве первичного стандарта используется оксалат натрия. Стандартизация производится при нагревании.
Другие сферы применения
[править | править код]- 1—2%-й раствор используется садоводами для протравливания семян перед посадкой[2]
- Применяется для определения перманганатной окисляемости при оценке качества воды согласно ГОСТ 2761-84 по методу Кубеля[3].
- Щелочной раствор перманганата калия хорошо отмывает лабораторную посуду от жиров и других органических веществ.
- Растворы (концентрации примерно 3 г/л) широко применяются при тонировании фотографий.
- В пиротехнике применяют в качестве сильного окислителя.
- Применяют в качестве катализатора разложения перекиси водорода в жидкостных ракетных двигателях.
- Водный раствор перманганата калия используется для травления дерева, в качестве морилки.
- Водный раствор применяется также для выведения татуировок. Результат достигается посредством химического ожога, при котором отмирают ткани, в которых содержится красящее вещество. Данный метод немногим отличается от простого срезания кожи, обычно он менее эффективен и более неприятен, так как ожоги заживают намного дольше. Татуировка не удаляется полностью, на её месте остаются шрамы.
- Перманганат калия или бихромат натрия используются в качестве окислителя при получении мета- и парафталевых кислот из мета- и параксилолов, соответственно (см. Терефталевая кислота).
- Перманганат калия является прекурсором в синтезе мефедрона и меткатинона (эфедрона).
Получение
[править | править код]Часто для получения небольших количеств, сплавляют диоксид марганца с нитратом или хлоратом калия и гидроксидом калия. Получающийся манганат(VI) калия далее либо окисляют хлором или электролизом, либо пропускают углекислый газ, создающий кисловатую (или примерно нейтральную) среду, в которой K2MnO4 дисмутирует, что, однако, уменьшает выход ввиду удаления марганца как MnO2.
Последняя реакция происходит при электролизе концентрированного раствора манганата калия и эндотермична, она является основным промышленным способом получения перманганата калия.
Ограничение на покупку
[править | править код]Входит в IV список прекурсоров ПККН в России[4] (допускается исключение некоторых мер контроля).
14 июня 2013 года на Украине был признан прекурсором и внесён в список наркотических веществ[5].
Примечания
[править | править код]- ↑ М. Д. Машковский. Лекарственные средства. — М.: ООО «Новая волна», 2002. — Т. 2. — 608 с. — 25 000 экз. — ISBN 5-7864-0129-4.
- ↑ Протравливание семян марганцовкой, приготовление раствора марганцовки. Как правильно развести марганцовку? — Всё о рассаде и теплицах. Дата обращения: 19 февраля 2019. Архивировано 25 февраля 2019 года.
- ↑ 6.2.6. Окисляемость, или химическое потребление кислорода (ХПК). www.anchem.ru. Дата обращения: 11 февраля 2023. Архивировано 1 апреля 2022 года.
- ↑ Постановление Правительства РФ от 30.06.1998 N 681 «Об утверждении перечня наркотических средств, психотропных веществ и их прекурсоров, подлежащих контролю в Российской Федерации» (с изменениями и дополнениями). Дата обращения: 27 марта 2014. Архивировано 20 апреля 2013 года.
- ↑ На Украине марганцовку признали прекурсором. Газета.Ru (14 июня 2013). Дата обращения: 14 июня 2013. Архивировано 18 июня 2013 года.
Литература
[править | править код]- Вульфсон Н. С. Препаративная органическая химия. — С. 656, 657.
- Казанский Б. А. (ред.). Синтезы органических препаратов (сборник 3). — С. 145.
- Реми Г. Курс неорганической химии (том 1). — С. 817.







![{\displaystyle {\ce {2KMnO4->[^{\circ }t]K2MnO4\ +MnO2\ +O2}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/9118731b5eb0575cae1da3c467a2d760f85453a5)
![{\displaystyle {\ce {5KMnO4->[^{\circ }t]K2MnO4\ +K3MnO4\ +3MnO2\ +3O2}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/9f9d3b8a183d05ee5073650c26e6bf2bc8ed4e66)











![{\displaystyle {\ce {3MnO2 + KClO3 + 6KOH ->[t] 3K2MnO4 + KCl + 3H2O}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/0df3170881ad196634407135db0ca290a5afd717)
![{\displaystyle {\ce {3K2MnO4 + 2H2O ->[H^+] 2KMnO4 + MnO2 v + 4KOH}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/c7b7d16e5f7c2d20314c94c542f27d877bffc42c)

