Лейкоциты

Лейкоци́ты (от др.-греч. λευκός — белый и κύτος — вместилище, тело; буквально белые клетки) — неоднородная группа различных по внешнему виду и функциям клеток крови человека и животных, выделенная по признакам наличия ядра и отсутствия самостоятельной окраски. Образуются в красном костном мозге, обнаруживаются во всём организме животного. Продолжительность жизни лейкоцита колеблется от нескольких часов до нескольких лет. Главная функция лейкоцитов — защита организма от патогенов и удаление продуктов разрушения тканей.
Лейкоциты подразделяют по признаку наличия гранул в цитоплазме на гранулоциты и агранулоциты или по происхождению в ходе гемопоэза на миелоидные и лимфоидные клетки. Эти широкие категории включают в себя более специализированные группы лейкоцитов: нейтрофилы, эозинофилы, базофилы, клетки системы мононуклеарных фагоцитов (моноциты, тканевые макрофаги, дендритные клетки) и лимфоциты. К клеткам миелоидного ряда относят нейтрофилы, эозинофилы, базофилы и клетки системы мононуклеарных фагоцитов, к клеткам лимфоидного — лимфоциты. Благодаря способности к фагоцитозу моноциты и нейтрофилы относят к фагоцитам.
Пониженное или повышенное количество лейкоцитов в крови служит важным индикатором наличия патологического процесса. В норме число лейкоцитов у взрослого человека находится в пределах от 4 × 109/л до 1,1 × 1010/л, что составляет около 1 % общего объёма крови. Повышение уровня лейкоцитов (лейкоцитоз) часто происходит при инфекциях, реже — при раковых и иных заболеваниях. Пониженный уровень лейкоцитов (лейкопения) свидетельствует об ослаблении иммунной системы.
Вещества, вызывающие реакцию воспаления, привлекают новые лейкоциты к месту внедрения чужеродных тел. Уничтожая чужеродные тела и поврежденные клетки, лейкоциты гибнут в больших количествах. Гной, который образуется в тканях при воспалении, — это скопление погибших лейкоцитов.
Виды лейкоцитов
[править | править код]По морфологическим признакам и биологическим функциям лейкоциты подразделяют на гранулоциты, или зернистые лейкоциты, и агранулоциты, или незернистые лейкоциты. Окрашивание гранулоцитов по Романовскому — Гимзе смесью кислого (эозин) и основного (азур II) выявляет в их цитоплазме наличие специфической зернистости (эозинофильной, базофильной или нейтрофильной у эозинофилов, базофилов, нейтрофилов соответственно), а также сегментированные ядра. Агранулоциты (моноциты и лимфоциты) имеют несегментированные ядра и не содержат цитоплазматических гранул. Процентное соотношение разных видов лейкоцитов в крови называют лейкоцитарной формулой, которая имеет важнейшее диагностическое значение[1].
Все лейкоциты — подвижные клетки, перемещающиеся с помощью псевдоподий. При движении лейкоцитов изменяется как форма самой клетки, так и форма её ядра, и лейкоциты могут проходить между клетками эндотелия и эпителия, преодолевать базальные мембраны и перемещаться по межклеточному матриксу соединительной ткани — именно в соединительной ткани они выполняют свои основные защитные функции. На скорость движения лейкоцитов влияют разнообразные химические и физические характеристики окружающей среды (температура, pH, химический состав и консистенция среды), а его направление определяется хемотаксисом под влиянием особых химических веществ (хемоаттрактантов). Главная функция лейкоцитов — защитная. Гранулоциты, в особенности, нейтрофилы и моноциты (а также их тканевая форма — макрофаги) способны к фагоцитозу и являются фагоцитами. Моноциты и макрофаги поглощают инородные вещества и продукты распада клеток и тканей, макрофаги и лимфоциты задействованы в иммунной защите[2].
Нейтрофилы
[править | править код]
Нейтрофилы — самые многочисленные лейкоциты крови, на их долю приходится 40—70 % всех лейкоцитов[3]. В мазках крови нейтрофилы имеют диаметр от 12 до 15 мкм. В суспензии человеческие нейтрофилы достигают 7—9 мкм в диаметре[4]. Ядро зрелoго сегментоядерного нейтрофила подразделено на 3—5 сегментов, также в кровотоке присутствует некоторое количество незрелых палочкоядерных нейтрофилов с несегментированным ядром. При окрашивании по Романовскому — Гимзе цитоплазма нейтрофилов окрашивается слабооксифильно. В цитоплазме содержатся специфические[англ.], азурофильные, секреторные и желатиназные[англ.] гранулы, которые содержат белки с антибактериальными свойствами: лактоферрин, щелочная фосфатаза, лизоцим, миелопероксидаза и другие, а также ферменты, генерирующие активные формы кислорода. После фагоцитоза бактерии нейтрофилом она оказывается внутри фагосомы, с которой сливаются гранулы нейтрофила, высвобождая бактерицидные и бактериостатические[англ.] компоненты[5].
Помимо фагоцитоза, антибактериальная активность нейтрофилов проявляется в виде особой формы программируемой клеточной гибели — нетоза. В ходе нетоза погибающий нейтрофил выбрасывает наружу хроматин вместе с бактерицидными белками, за счет чего клетки патогенов обездвиживаются и подвергаются действию антибактериальных белков[6].
Нейтрофилы экспрессируют и продуцируют широкий спектр цитокинов, среди которых хемокины, колониестимулирующие факторы[англ.], провоспалительные цитокины[англ.] (IL-1α, IL-1β, IL-6, IL-7, IL-18, MIF[англ.] и другие), иммунорегуляторные цитокины (IL-12, IL-21[англ.], IL-23[англ.], IL-27[англ.], TSLP[англ.] и другие), противовоспалительные цитокины (IL-1ra, TGFβ1, TGFβ2[англ.]), факторы ангиогенеза и фиброгенеза (VEGF, BV8, HBEGF[англ.], FGF2[англ.], TGFα[англ.], HGF[англ.], ангиопоэтин), цитокины суперсемейства фактора некроза опухоли (TNF) и некоторые другие цитокины, такие как PBEF, амфирегулин[англ.], мидкин, онкостатин M[англ.], активин A[англ.], эндотелин. За счёт выделения разнообразных цитокинов нейтрофилы могут быть вовлечены в процессы, не связанные с иммунной защитой, такие как гемопоэз, ангиогенез и заживление ран. Кроме того, нейтрофилы могут участвовать в развитии некоторых аутоиммунных и злокачественных заболеваний[7].
Базофилы
[править | править код]
Базофилы являются разновидностью лейкоцитов, которые участвуют в развитии аллергических реакций. Своё название базофилы получили из-за наличия в цитоплазме базофильных гранул. У человека доля базофилов от числа лейкоцитов в крови составляет 0,5 %. Диаметр базофилов в мазке крови составляет 11—12 мкм, в капле крови — 9 мкм[8]. Морфологически базофилы близки не только к другим гранулоцитам, но и к тучным клеткам, с которыми они тесно связаны функционально[9].
Базофильные гранулы, находящиеся в цитоплазме базофилов, содержат гистамин, протеазы химазу[англ.] и триптазу, некоторые другие ферменты, протеогликаны (преимущественно хондроитинсульфаты) и гликозаминогликаны. Базофилы секретируют сравнительно немного активных веществ: лейкотриен C3, интерлейкины IL-4 и IL-13[англ.] и некоторые другие цитокины[9].
Вместе с эозинофилами и нейтрофилами они мигрируют в очаг аллергического воспаления из кровотока. Связывание иммуноглобулинов E с Fc-рецепторами на базофилах активирует их, и базофилы начинают выделять наружу содержимое гранул. Высвобождение содержимого гранул базофилов обеспечивает поддержание аллергического процесса, инициированного тучными клетками[9].
Эозинофилы
[править | править код]
Основная функция эозинофилов заключается в борьбе с многоклеточными паразитами, кроме того, они участвуют в развитии аллергических реакций. Эозинофилы — довольно крупные клетки, достигают от 18 до 20 мкм в диаметре. Зрелые эозинофилы имеют ядро, разделённое на две части (двудольное), и крупные эозинофильные гранулы до 1 мкм в диаметре, содержащие белки с цитотоксическими свойствами. У здорового человека эозинофилы составляют от 0,5 % до 2 % от общего числа лейкоцитов[10].
Эозинофильность гранул в цитоплазме эозинофилов достигается за счёт главного щелочного белка[англ.] (англ. major basic protein, MBP). Главная роль эозинофилов заключается в борьбе с многоклеточными паразитами за счёт внеклеточного цитолиза их клеток. Многие белки, входящие в состав гранул эозинофилов, обладают токсичностью в отношении гельминтов: так, эозинофильный катионный белок встраивается в мембраны их клеток, нарушая их целостность. Эозинофильный катионный белок[англ.] (англ. eosinophilic cationic protein, ECP) и происходящий от эозинофилов нейротоксин[англ.] (англ. eosinophil-derived neurotoxin, EDN) являются РНКазами, а потому играют роль в противовирусной защите. MBP принимает участие в активации тучных клеток и базофилов, поэтому эозинофилы задействованы в развитии аллергических реакций. Кроме того, эозинофилы обладают регулирующей активностью, так как действуют на T-лимфоциты (T-клетки). Эозинофилы задействованы в положительной селекции T-клеток в тимусе, но их роль в этом процессе изучена плохо. Эозинофилы также обладают слабой фагоцитарной активностью. Помимо функций в иммунной системе, эозинофилы регулируют морфогенетические процессы, связанные с половым циклом самок и беременностью[11].
Эозинофилы, подобно другим иммунным клеткам, выделяют разнообразные цитокины, которые, в частности, участвуют в активации T-хелперов типа Th2. Эозинофилы секретируют широкий спектр цитокинов, в их числе IL-2, IL-3, IL-4, IL-5, IL-6, IL-8, IL-10, IL-12[англ.], IL-13[англ.], IL-16[англ.], IL-18, TNFα[англ.], IFNγ, TGFβ, GM-CSF. Помимо того, эозинофилы выделяют некоторые хемокины (эотаксин[англ.] ССL11[англ.], RANTES[англ.] (ССL5), MIP-1α[англ.] (ССL3)), эйкозаноиды (лейкотриены, фактор агрегации тромбоцитов (PAF)) и нейропептиды[12].
Клетки системы мононуклеарных макрофагов
[править | править код]
Моноциты, циркулирующие в кровотоке, резидентные макрофаги, локализованные в тканях, и дендритные клетки составляют систему мононуклеарных макрофагов, также известную как ретикулоэндотелиальная система. Эти клетки задействованы не только в работе иммунной системы: они также участвуют в развитии организма (онтогенезе) и удалении продуктов разрушения тканей[13].
У взрослого человека на долю моноцитов приходится 6—8 % общего числа лейкоцитов крови, кроме того, моноциты присутствуют в крови и селезёнке. Моноциты крупнее прочих лейкоцитов: в капле крови их диаметр составляет 9—12 мкм, а в мазке они сильно распластываются, и их диаметр достигает 18—20 мкм[14]. После выхода в кровь моноциты циркулируют в кровотоке 1—2 дня, после чего оседают в тканях и становятся резидентными макрофагами. Тем не менее моноциты сами по себе являются клетками врождённого иммунитета и несут патогенраспознающие рецепторы и рецепторы хемокинов[англ.], благодаря которым они могут перемещаться в очаг воспаления, где они секретируют провоспалительные цитокины и участвуют в фагоцитозе. Находясь в очаге воспаления, моноциты дифференцируются в воспалительные макрофаги и воспалительные дендритные клетки[15].
Часть макрофагов локализуется в определённых участках лимфоидной ткани, таких как медуллярные тяжи лимфатических узлов, красная[англ.] и белая пульпа[англ.] селезёнки. Кроме того, существуют тканевые макрофаги, которые обнаруживаются во всех нелимфоидных органах, где их численность может достигать 10—15 % общего числа клеток. К тканевым макрофагам относятся клетки Купфера в печени, остеокласты костной ткани, микроглия нервной ткани, гистиоциты[англ.] соединительной ткани, клетки Лангерганса кожи, альвеолярные макрофаги[англ.], мезангиальные клетки[англ.] почек, макрофаги слизистых оболочек и серозных полостей, поджелудочной железы, интерстициальной ткани сердца. Макрофаги поддерживают гомеостаз тканей, очищают организм от стареющих и погибших клеток, восстанавливают ткани после повреждений и инфекций. Макрофаги задействованы в работе врождённого иммунитета и несут паттернраспознающие рецепторы, а также обладают разнообразными механизмами уничтожения поглощённых клеток патогенов[16].
Дендритные клетки, получившие своё название из-за наличия отростков, широко представлены в организме. Они многочисленны в покровных тканях, носоглотке, лёгких, кишечнике, желудке, лимфоидных органах, а их незрелые формы присутствуют в кровотоке. Единственная функция дендритных клеток заключается в презентации антигенов и передаче стимулирующих сигналов лимфоцитам. Дендритные клетки захватывают экзогенные антигены, осуществляют его процессинг[англ.] и выставляют фрагменты антигена на своей поверхности в комплексе с молекулами главного комплекса гистосовместимости II класса[англ.] (или I класса[англ.] в случае кросс-презентации[англ.]). В таком виде антиген может быть узнан T-клеточным рецептором. По происхождению дендритные клетки подразделяют на миелоидные, происходящие от моноцитов, и плазмоцитоидные, которые происходят от общей лимфоидной клетки-предшественника[17].
Лимфоциты
[править | править код]
У взрослого человека лимфоциты составляют 20—35 % всех лейкоцитов. По размеру лимфоциты подразделяют на малые (диаметром 4,5—6 мкм), средние (диаметром 7—10 мкм) и большие (диаметром 10 мкм и более). Большие лимфоциты присутствуют только у новорождённых и детей, у взрослых 85—90 % составляют малые лимфоциты. Лимфоциты имеют интенсивно окрашенное округлое или бобовидное ядро и относительно узкую прослойку базофильной цитоплазмы[18].
Функционально лимфоциты относятся к адаптивной иммунной системе. Лимфоциты — единственный тип клеток в организме млекопитающих, дифференцировка которых сопровождается значительными перестройками генов, кодирующих антигенраспознающие рецепторы. По функциям и строению антиген-распознающих рецепторов лимфоциты подразделяют на T-лимфоциты и B-лимфоциты, также к лимфоцитам относят естественные киллеры, NKT-клетки[англ.] и некоторые другие группы иммунных клеток. Связывание антигенраспознающего рецептора лимфоцита с антигеном необходимо, но ещё недостаточно для запуска иммунного ответа. Помимо антигенраспознающих рецепторов, лимфоциты несут корецепторы, активация которых также необходима для развития иммунного ответа. Лимфоциты распознают антиген либо в нативном состоянии (B-лимфоциты), либо в модифицированном виде на поверхности антигенпрезентирующих клеток (T-лимфоциты). Запуск адаптивного иммунного ответа сопровождается дифференцировкой B-лимфоцитов в плазматические клетки, производящие антитела, в лимфоидных органах. T-клетки, как и B-клетки, выходят из кровотока и мигрируют в очаг воспаления, где непосредственно разрушают заражённые клетки или выделяют цитокины, стимулирующие другие лейкоциты, в том числе макрофаги, эозинофилы и естественные киллеры[19].
Фагоцитоз
[править | править код]
Важнейшая функция лейкоцитов — фагоцитоз, то есть поглощение клеткой крупных макромолекулярных комплексов или частиц. Главной функцией фагоцитоз является у четырёх групп лейкоцитов, которые называют «профессиональными» фагоцитами: нейтрофилов, моноцитов, макрофагов и дендритных клеток. Фагоцитоз начинается с миграции лейкоцитов из кровотока в очаг воспаления под действием хемоаттрактантов (хемотаксис), распознавания клеток патогенов и их прикрепления к лейкоцитам. Далее лейкоцит поглощает микроорганизм, и он оказывается внутри вакуоли — фагосомы, с которой сливаются гранулы лейкоцитов, несущие антибактериальные компоненты, в результате чего образуется фаголизосома[англ.]. В фаголизосоме образуются активные формы кислорода и азота (окислительный взрыв[англ.]), под их действием, а также под действием ферментов гранул микроорганизм погибает. Продукты разрушения микрорганизма выбрасываются наружу в ходе экзоцитоза, во время которого мембрана фаголизосомы встраивается обратно в клеточную мембрану. В случае макрофагов и дендритных клеток продукты расщепления антигенов, несомых микроорганизмов, презентируются T-лимфоцитам[20].
Проникновение лейкоцита из кровеносного сосуда в ткань наиболее изучено в случае нейтрофилов и включает стадии качения (роллинга), адгезии, распластывания и диапедеза. В ходе роллинга нейтрофил обратимо связывается с клетками эндотелия за счёт связывания селектинов эндотелиоцитов с гликопротеинами на поверхности лейкоцита. Адгезия включает в себя прочное присоединения нейтрофила к эндотелию за счёт связывания интегринов нейтрофила с иммуноглобулиноподобными[англ.] молекулами на поверхности эндотелия. Эти взаимодействия запускают перестройку цитоскелета нейтрофила, из-за которой происходит его распластывание. Диапедез заключается в проникновении нейтрофила между эндотелиоцитами за счёт взаимодействия специальных молекул на нейтрофиле и клетках эндотелия, а также за счёт выделения нейтрофилом металлопротеиназ[англ.], расщепляющих перемычки между эндотелиоцитами[21].
Развитие
[править | править код]
Миелопоэз, в ходе которого образуются эритроциты, моноциты, гранулоциты, тромбоциты и предшественники моноцитов, происходит в миелоидной ткани[англ.], которую составляет красный костный мозг, залегающий в эпифизах трубчатых и полостях многих губчатых костей. Предшественники лимфоцитов из костного мозга мигрируют в лимфоидную ткань, расположенную в тимусе, селезёнке, лимфатических узлах[22].
Все форменные элементы происходят из популяции плюрипотентных стволовых кроветворных клеток, находящейся в костном мозге. Существуют две линии дифференцировки стволовых кроветворных клеток. Одна линия даёт начало мультипотентной[англ.] клетке-родоначальнице гранулоцитарного, эритроцитарного, моноцитарного и мегакариоцитарного рядов гемопоэза (эту клетку обозначают КОЕ-ГЭММ). Из второй линии происходит мультипотентная клетка-родоначальница лимфопоэза (КОЕ-Л). КОЕ-ГЭММ и КОЕ-Л дают начало олигопотентным и, далее, унипотентным клеткам-предшественницам. Гранулоциты и моноциты происходят от общей олигопотентной клетки КОЕ-ГМ. Моноциты, нейтрофилы, эозинофилы и базофилы происходят от соответствующих унипотентных клеток — КОЕ-М, КОЕ-Гн, КОЕ-Эо, КОЕ-Б. Плюрипотентные, мультипотентные, олигопотентные и унипотентные клетки-предшественницы морфологически неразличимы[23].
В развитии гранулоцитов (гранулопоэз) после стадии унипотентной клетки следует стадия миелобластов, которые дают начало промиелоцитам — клеткам с базофильной цитоплазмой, на стадии которых начинают появляться азурофильные гранулы. Из промиелоцитов образуются миелоциты, на стадии которых в цитоплазме появляются специфические гранулы и характерная для данного типа гранулоцитов зернистость. Миелоциты дают начало метамиелоцитам, которые, в отличие от клеток всех предыдущих стадий, не делятся. Метамиелоциты дают начало лейкоцитам — юным палочкоядерным и зрелым сегментоядерным. Все миелоциты, особенно дающие начало нейтрофилам, обладают выраженной фагоцитарной активностью, а на стадии метамиелоцита приобретают подвижность[24].
Лейкоциты беспозвоночных
[править | править код]
У беспозвоночных животных лейкоциты (амёбоциты) содержатся в крови, гемолимфе и полостной жидкости. Наиболее многочисленная группа фагоцитов, имеющаяся у многих беспозвоночных, — крупные базофильные незернистые амёбоциты. Они способны к амебоидному движению и демонстрируют положительный хемотаксис к чужеродным поверхностям. Фагоциты беспозвоночных подробно описал Илья Ильич Мечников. Помимо незернистых амёбоцитов, у некоторых беспозвоночных, в частности, у полухордовых, имеется система гранулярных амёбоцитов. В их цитоплазме имеются многочисленные гранулы, а также особые микротрубочковые структуры диаметром 15—20 мкм. По химическому составу гранулы можно разделить на две группы. Гранулы первой группы имеются у амёбоцитов насекомых, ракообразных, асцидий, стрекающих и, вероятно, иглокожих. Эти гранулы содержат мономеры белка, способного к полимеризации, неактивный фермент, запускающий его полимеризацию, фенолы и неактивную в гранулах фенолоксидазу[англ.], а также мукополисахаридный матрикс, поддерживающий неактивное состояние в гранулах указанных ферментов. Активация происходит во время высвобождения содержимого гранул путём экзоцитоза, при этом мономерный белок полимеризуется и формирует плёнку, которую укрепляют хиноны, образующиеся при окислении фенолов фенолоксидазой. Функции гранулярных амёбоцитов различны в разных группах животных. Так, у асцидий благодаря формированию плёнки укрепляется вещество туники[англ.], у насекомых они участвуют в закупорке отверстий в наружных покровах, у ракообразных они обеспечивают инкапсуляцию гиф паразитических грибов. Гранулы второй группы, обнаруженные у приапулид и мечехвостов, не содержат фенолов и фенолоксидазы. У этих животных гранулярные амёбоциты обеспечивают свёртывание гемолимфы и защиту от чужеродных агентов[25].
Клиническое значение
[править | править код]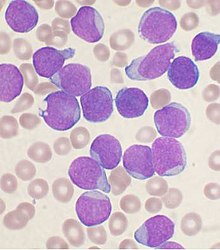
Состояние, при котором количество лейкоцитов в крови становится менее 4000 в 1 мкл, называется лейкопенией. Чаще всего лейкопения обусловлена снижением количества нейтрофилов в крови — нейтропенией. Причины лейкопении разнообразны. Лейкопения может развиваться под действием ионизирующего излучения, ряда химических веществ (бензола, соединений мышьяка, ДДТ), некоторых лекарственных препаратов (цитостатические препараты, антитиреоидные агенты[англ.], ряд антибиотиков). Лейкопения может возникать как следствие вирусных инфекций, тяжёлых бактериальных инфекций, малярии, коллагенозов. Снижение уровня лейкоцитов также происходит при некоторых заболеваниях крови, таких как гипопластическая анемия и пароксизмальная ночная гемоглобинурия, а также в результате спленэктомии и при острых анафилактических реакциях[26]. Снижение количества лимфоцитов до уровня ниже 1000 в мкл крови известно как лимфоцитопения[англ.] или лимфопения. Как правило, лимфопения обусловлена падением уровня T-лимфоцитов[27].
Повышение содержания лейкоцитов в крови до 10 000 и более в мкл известно как лейкоцитоз. Резкое повышение уровня лейкоцитов до 20 000 в мкл крови называют гиперлейкоцитозом. Как правило, лейкоцитоз связан с увеличением количества нейтрофилов. Повышение содержания нейтрофилов в крови происходит как при нормальных физиологических реакциях (стресс, приём пищи и другие), так и при патологических процессах: инфекциях, интоксикациях, появлении злокачественных новообразований и других. Нейтрофилы в большом количестве содержатся в гное[28]. Повышение уровня эозинофилов в крови наблюдается при аллергических реакциях немедленного типа, бронхиальной астме, эозинофильной пневмонии, миелоидном лейкозе[англ.], а также при синдроме Лёффлера[англ.]. Содержание базофилов в крови выше нормы поднимается редко. Базофильный лейкоцитоз может наблюдаться при микседеме, неспецифическом язвенном колите, аллергических реакциях, а также во время беременности. Увеличение уровня лимфоцитов в крови наблюдается при некоторых острых и хронических инфекциях: коклюше, туберкулёзе, сифилисе, бруцеллёзе, инфекционном мононуклеозе. Моноцитарный лейкоцитоз — редкое состояние, оно может наблюдаться при бактериальных и протозойных инфекциях, а также при раковых заболеваниях, саркоидозе и коллагенозах[29].
Нарушения гемопоэза, отражающиеся на количестве и некоторых свойствах лейкоцитов, часто сопровождают гемобластозы — злокачественные преобразования клеток крови, костного мозга, лимфы и лимфоидной ткани. Опухоли, сопровождающиеся избыточным количеством клеток миелоидного происхождения, известны как миелопролиферативные неоплазии[англ.]. К их числу относят, в частности, хронический миелоидный лейкоз, хронический нейтрофильный лейкоз[англ.] и хронический эозинофильный лейкоз[англ.][30]. Чрезмерная пролиферация лимфоидных клеток происходит при таких неоплазиях, как фолликулярная лимфома[31], хронический лимфолейкоз[32], острый лимфобластный лейкоз[33] и миеломная болезнь[34].
История изучения
[править | править код]
Изучение форменных элементов крови стало возможным после изобретения сложного микроскопа Захарием Янсеном около 1590 года. Хотя эритроциты были описаны ещё в 1658 году, лейкоциты долго оставались без внимания исследователей из-за своей относительной, по сравнению с эритроцитами, немногочисленности и прозрачности. Первое описание белых клеток крови выполнил французский врач Жозеф Льето в 1749 году в посмертном материале, и в том же году другой французский доктор, Жан Батист Сенак, открыл белые клетки в составе гноя. Первое подробное описание форменных элементов крови и лимфы выполнил английский хирург Уильям Хьюсон[англ.] в 1773 году. Он отметил, что белые клетки крови гораздо менее многочисленны по сравнению с красными. Кровь больного лейкозом впервые описал Альфред Франсуа Донне[англ.] в 1839 году, отметив резкое увеличение количество в ней белых клеток. В 1843 году Уильям Эддисон[англ.] показал, что белые клетки, входящие в состав гноя, происходят от лейкоцитов крови. В 1863 году ассистент Рудольфа Вирхова Фридрих Даниель фон Реклингхаузен описал амёбоидные свойства лейкоцитов — подвижность и способность к формированию псевдоподий. Чуть позднее Юлиус Фридрих Конгейм показал, что лейкоциты могут проникать через стенки капилляров за счёт амёбоидного движения. В 1879 году Пауль Эрлих разработал методы окрашивания клеток крови и выполнил их детальные морфологические описания. Кислые и основные красители, разработанные Эрлихом, позволили описать эозинофилы, нейтрофилы, базофилы и лимфоциты[35]. Фагоцитоз был детально изучен и назван Ильёй Ильичом Мечниковым в 1882 году, когда им же была установлена роль фагоцитов в защите от бактерий[36]. В 1908 году Пауль Эрлих и Илья Мечников разделили Нобелевскую премию по физиологии и медицине[37].
Примечания
[править | править код]- ↑ Афанасьев и др., 2004, с. 176.
- ↑ Афанасьев и др., 2004, с. 175—176.
- ↑ Actor Jeffrey K. Cells and Organs of the Immune System (англ.) // Elsevier's Integrated Review Immunology and Microbiology. — 2012. — P. 7—16. — ISBN 9780323074476. — doi:10.1016/B978-0-323-07447-6.00002-8.
- ↑ Niemiec M. J., De Samber B., Garrevoet J., Vergucht E., Vekemans B., De Rycke R., Björn E., Sandblad L., Wellenreuther G., Falkenberg G., Cloetens P., Vincze L., Urban C. F. Trace element landscape of resting and activated human neutrophils on the sub-micrometer level. (англ.) // Metallomics : Integrated Biometal Science. — 2015. — June (vol. 7, no. 6). — P. 996—1010. — doi:10.1039/c4mt00346b. — PMID 25832493.
- ↑ Афанасьев и др., 2004, с. 176—178.
- ↑ Хаитов, 2019, с. 74.
- ↑ Tecchio C., Micheletti A., Cassatella M. A. Neutrophil-derived cytokines: facts beyond expression. (англ.) // Frontiers In Immunology. — 2014. — Vol. 5. — P. 508—508. — doi:10.3389/fimmu.2014.00508. — PMID 25374568.
- ↑ Афанасьев и др., 2004, с. 180.
- ↑ 1 2 3 Ярилин, 2010, с. 62.
- ↑ Ярилин, 2010, с. 57.
- ↑ Ярилин, 2010, с. 57—58.
- ↑ Ярилин, 2010, с. 58.
- ↑ Хаитов, 2019, с. 77—78.
- ↑ Афанасьев и др., 2004, с. 184.
- ↑ Хаитов, 2019, с. 78.
- ↑ Хаитов, 2019, с. 79—81.
- ↑ Хаитов, 2019, с. 192—194.
- ↑ Афанасьев и др., 2004, с. 181.
- ↑ Хаитов, 2019, с. 94—96.
- ↑ Хаитов, 2019, с. 68.
- ↑ Хаитов, 2019, с. 69.
- ↑ Афанасьев и др., 2004, с. 194.
- ↑ Афанасьев и др., 2004, с. 194—195.
- ↑ Афанасьев и др., 2004, с. 203—204.
- ↑ Заварзин, 1985, с. 242—246.
- ↑ Большая медицинская энциклопедия: ЛЕЙКОПЕНИЯ. Дата обращения: 27 сентября 2020. Архивировано 4 марта 2021 года.
- ↑ Lymphocytopenia. National Heart, Lung and Blood Institute. NIH. Дата обращения: 10 февраля 2020. Архивировано 12 марта 2020 года.
- ↑ Mescher, 2016, p. 243—244.
- ↑ Большая медицинская энциклопедия: ЛЕЙКОЦИТОЗ. Дата обращения: 27 сентября 2020. Архивировано 30 сентября 2020 года.
- ↑ Arber D. A., Orazi A., Hasserjian R., Thiele J., Borowitz M. J., Le Beau M. M., Bloomfield C. D., Cazzola M., Vardiman J. W. The 2016 revision to the World Health Organization classification of myeloid neoplasms and acute leukemia. (англ.) // Blood. — 2016. — 19 May (vol. 127, no. 20). — P. 2391—2405. — doi:10.1182/blood-2016-03-643544. — PMID 27069254.
- ↑ Xerri L., Dirnhofer S., Quintanilla-Martinez L., Sander B., Chan J. K., Campo E., Swerdlow S. H., Ott G. The heterogeneity of follicular lymphomas: from early development to transformation. (англ.) // Virchows Archiv : An International Journal Of Pathology. — 2016. — February (vol. 468, no. 2). — P. 127—139. — doi:10.1007/s00428-015-1864-y. — PMID 26481245.
- ↑ Boelens J., Lust S., Vanhoecke B., Offner F. Chronic lymphocytic leukaemia. (англ.) // Anticancer Research. — 2009. — February (vol. 29, no. 2). — P. 605—615. — PMID 19331210.
- ↑ Childhood Acute Lymphoblastic Leukemia Treatment (англ.). National Cancer Institute (8 декабря 2017). Дата обращения: 20 декабря 2017. Архивировано 10 июня 2021 года.
- ↑ Raab M. S., Podar K., Breitkreutz I., Richardson P. G., Anderson K. C. Multiple myeloma. (англ.) // Lancet (London, England). — 2009. — 25 July (vol. 374, no. 9686). — P. 324—339. — doi:10.1016/S0140-6736(09)60221-X. — PMID 19541364.
- ↑ Kay A. B. Paul Ehrlich and the Early History of Granulocytes. (англ.) // Microbiology Spectrum. — 2016. — August (vol. 4, no. 4). — doi:10.1128/microbiolspec.MCHD-0032-2016. — PMID 27726791.
- ↑ Gordon S. Phagocytosis: An Immunobiologic Process. (англ.) // Immunity. — 2016. — 15 March (vol. 44, no. 3). — P. 463—475. — doi:10.1016/j.immuni.2016.02.026. — PMID 26982354.
- ↑ The Nobel Prize in Physiology or Medicine 1908, Paul Erlich - Biography. Дата обращения: 27 сентября 2020. Архивировано 14 августа 2018 года.
Литература
[править | править код]- Афанасьев Ю. И., Кузнецов С. Л., Юрина Н. А., Котовский Е. Ф. и др. Гистология, цитология и эмбриология. — 6-е изд., перераб. и доп.. — М.: Медицина, 2004. — 768 с. — ISBN 5-225-04858-7.
- Заварзин А. А. Основы сравнительной гистологии. — Л.: Издательство Ленинградского университета, 1985. — 400 с.
- Хаитов Р. М. Иммунология: структура и функции иммунной системы. — М.: ГЭОТАР-Медиа, 2019. — 328 с. — ISBN 978-5-9704-4962-2.
- Ярилин А. А. Иммунология. — М.: ГЭОТАР-Медиа, 2010. — 752 с. — ISBN 978-5-9704-1319-7.
- Anthony L. Mescher. Junqueira's Basic Histology. — McGraw-Hill Education, 2016. — ISBN 978-0-07-184270-9.
Эта статья входит в число избранных статей русскоязычного раздела Википедии. |