Хронический лимфолейкоз
| Хронический лимфолейкоз | |
|---|---|
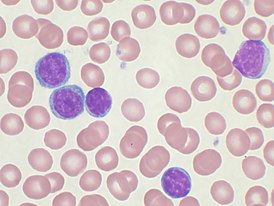 Злокачественные клетки в мазке периферической крови | |
| МКБ-11 | XH15T2 |
| МКБ-10 | C91.1 |
| МКБ-10-КМ | C91.1 и C91.10 |
| МКБ-9 | 204.9 |
| МКБ-9-КМ | 204.1[1][2] |
| МКБ-О | 9823/3 |
| OMIM | 151400, 609630, 109543, 612557, 612559 и 612558 |
| DiseasesDB | 2641 |
| MedlinePlus | 000532 |
| eMedicine | med/370 |
| MeSH | D015462 |
Хронический лимфолейкоз, или хронический лимфоцитарный лейкоз (ХЛЛ), — злокачественное клональное лимфопролиферативное заболевание, характеризующееся накоплением атипичных зрелых CD5/CD19/CD23-положительных В-лимфоцитов преимущественно в крови, костном мозге, лимфатических узлах, печени и селезёнке[3].
Эпидемиология
[править | править код]Хронический лимфолейкоз — одно из наиболее распространённых онкогематологических заболеваний[4]. Также это наиболее частый вариант лейкоза среди представителей европеоидной расы. По непонятным причинам редко встречается среди населения стран Восточной Азии. Дебют заболевания, как правило, происходит в пожилом возрасте — медианный возраст на момент постановки диагноза составляет 70—72 года. Мужчины болеют в 1,5—2 раза чаще, чем женщины. Ежегодная заболеваемость составляет 6,8 случая на 100 тыс. мужчин и 3,5 случая на 100 тыс. женщин[5].
Предрасположенность к заболеванию передаётся по наследству — риск развития хронического лимфоцитарного лейкоза у непосредственных родственников в 8,5 раз превышает популяционный, однако даже при этом остается ниже 1 %[6]. Описаны семейные случаи с относительно высокой пенетрантностью. Большей части случаев ХЛЛ, если не всем, предшествует предлейкозное состояние (моноклональный В-клеточный лимфоцитоз), которое наблюдается у 5—10 % людей в возрасте старше 40 лет и прогрессирует в ХЛЛ с частотой около 1 % в год[7].
Этиология
[править | править код]Наследственные факторы
[править | править код]Анализ генома людей с наследственным ХЛЛ позволил идентифицировать однонуклеотидные полиморфизмы, ассоциированные с этим состоянием. Полиморфизмы были обнаружены примерно в 30 локусах, например, в генах IRF4, ''LEF1''[англ.] и BCL2[5].
Факторы окружающей среды
[править | править код]Контакт с агентом «оранж»[8] и инсектицидами[9] могут повышать риск развития ХЛЛ.
Этиологическая связь ХЛЛ с ионизирующим излучением, вирусными инфекциями, питанием и образом жизни не доказана[5].
Патогенез
[править | править код]Первоначально хронический лимфоцитарный лейкоз рассматривали как онкологическое заболевание, характеризующееся накоплением долгоживущих, но очень редко делящихся иммунологически некомпетентных B-лимфоцитов[10]. Однако исследования с использованием тяжёлой воды показали, что злокачественные клетки пролиферируют, и достаточно быстро — количество новых клеток, образующихся за день, составляет от 0,1 до более чем 1 % от общего числа клеток клона[11]. Причём при высокой скорости пролиферации более вероятно агрессивное течение болезни.
Клеточное микроокружение (ниша) играет большую роль в патогенезе хронического лимфолейкоза. Пролиферация злокачественных клеток происходит в микроанатомических структурах, которые называются пролиферативными центрами, или псевдофолликулами. Псевдофолликулы представляют собой скопления лейкозных клеток, находящихся в контакте со вспомогательными клетками (например, стромальными клетками), которые стимулируют их пролиферацию и выживание[12]. Пролиферативные центры в основном находятся в лимфатических узлах и в меньшей степени в костном мозге[13].
Происхождение злокачественного клона
[править | править код]Злокачественные клетки имеют CD19/CD5/CD23-положительный иммунофенотип и низкий уровень мембранных иммуноглобулинов. Нормальные популяции В-клеток с таким набором поверхностных маркеров неизвестны, что мешает установить, какой тип клеток может давать начало злокачественному клону при ХЛЛ. Анализ транскриптома показал, что опухолевые клетки по набору синтезируемых мРНК похожи на зрелые В-клетки, которые прошли активацию антигеном. В норме таким профилем экспрессии генов обладают В-клетки памяти и В-клетки краевой зоны лимфатических фолликулов, поэтому предполагают, что именно они могут быть предшественниками лейкозных клеток[7].
В отличие от других B-клеточных лейкозов, для ХЛЛ не удалось выявить типичных хромосомных транслокаций, затрагивающих онкогены. Кроме того, крупные хромосомные перестройки редко наблюдаются на ранних стадиях заболевания, так что маловероятно, что они являются первичной причиной ХЛЛ. Однако по мере прогрессирования заболевания такие перестройки происходят: чаще всего это делеции участков хромосом 11, 13 и 17[3].
Клинические проявления
[править | править код]Характерен абсолютный лимфоцитоз в периферической крови (по данным гемограммы) и костном мозге (по данным миелограммы). На ранних стадиях лимфоцитоз является единственным проявлением заболевания. Пациенты могут предъявлять жалобы на так называемые «конституциональные симптомы» — астению, повышенную потливость, спонтанное снижение массы тела.
Характерна генерализованная лимфаденопатия. Увеличение внутригрудных и внутрибрюшных лимфатических узлов выявляется при ультразвуковом или рентгенологическом обследовании, периферические лимфоузлы доступны пальпации. Лимфатические узлы могут достигать значительных размеров, образовывать мягкие или плотноватые конгломераты. Сдавление внутренних органов не характерно.
На более поздних стадиях заболевания присоединяется гепатомегалия и спленомегалия. Увеличение селезёнки может проявляться ощущением тяжести или дискомфорта в левом подреберье, феноменом раннего насыщения.
За счёт накопления опухолевых клеток в костном мозге и вытеснения нормального гемопоэза на поздних стадиях могут развиваться анемия, тромбоцитопения, редко нейтропения. Поэтому пациенты могут жаловаться на общую слабость, головокружения, петехии, экхимозы, спонтанную кровоточивость.
Анемия и тромбоцитопения также могут иметь аутоиммунный генез.
Для заболевания характерна выраженная иммуносупрессия, затрагивающая преимущественно гуморальный иммунитет (гипогаммаглобулинемия). Из-за этого имеется предрасположенность к инфекциям, например, рецидивирующим простудным заболеваниям и пневмонии.
Необычным клиническим проявлением заболевания может быть гиперреактивность на укусы насекомых.
Диагностика
[править | править код]Для дифференциальной диагностики хронического лимфоцитарного лейкоза с другими лимфопролиферативными заболеваниями необходимо проанализировать количество В-клеток в периферической крови, мазок крови и провести иммунофенотипирование циркулирующих в крови лимфоцитов. Дополнительно для определения прогноза (но не схемы лечения) иногда проводят цитогенетическое исследование, определяют мутационный статус локуса IgVH, количество ZAP-70 или CD38 в клетках ХЛЛ, количество CD23, тимидинкиназы и β2-микроглобулина в сыворотке крови, а также анализируют биоптат или аспират костного мозга[14].
Анализ крови
[править | править код]
Необходимым критерием диагноза хронического лимфоцитарного лейкоза является повышение абсолютного числа В-лимфоцитов в крови до или более 5×109/л. Кроме того, эти лимфоциты должны иметь характерный иммунофенотип: на их поверхности должны обнаруживаться CD19, CD5, CD23, небольшие количества CD20 и CD79b, а также лёгкие цепи иммуноглобулинов[15].
В мазке крови обнаруживаются опухолевые клетки, которые имеют морфологию зрелых (малых) лимфоцитов: «штампованное» ядро с конденсированным хроматином без ядрышка, узкий ободок цитоплазмы. Характерно наличие так называемых теней Гумпрехта, которые представляют собой лейкозные клетки, разрушившиеся в процессе приготовления мазка. Помимо малых лимфоцитов в мазке могут присутствовать более крупные или атипичные клетки, иногда отмечается существенная (более 10 %) примесь омоложённых клеток (пролимфоцитов и параиммунобластов), требующая проведения дифференциального диагноза с пролимфоцитарным лейкозом[14].
Иммунофенотипирование
[править | править код]Иммунофенотипирование лимфоцитов методом проточной цитометрии обязательно для подтверждения диагноза. Высокочувствительная проточная цитометрия позволяет обнаруживать одну злокачественную клетку на 10 000 нормальных лейкоцитов[15]. В качестве диагностического материала обычно используется периферическая кровь. Для клеток ХЛЛ характерен аберрантный иммунофенотип: одновременная экспрессия (коэкспрессия) Т-клеточного маркера CD5 и В-клеточных маркеров CD19 и CD23[14]. Количество В-клеточных маркеров CD20, CD79b и мембраносвязанных иммуноглобулинов IgM и IgD понижено по сравнению с нормальными В-клетками[3]. В дополнение к этому выявляется клональность. Диагноз ХЛЛ также может быть установлен на основании данных иммуногистохимического исследования биоптата лимфатического узла или селезёнки.
Подозрение на хронический лимфоцитарный лейкоз также возникает в случае обнаружения у в остальном здоровых людей увеличения абсолютного числа клональных B-лимфоцитов соответствующего иммунофенотипа, даже если общее их количество в периферической крови меньше 5000/микролитр. Если этому признаку не сопутствует лимфаденопатия или органомегалия, цитопении или другие признаки заболевания, такое состояние диагностируется как моноклональный B-лимфоцитоз[14]. Согласно исследованию, проведённому на 1520 участниках в возрасте от 62 до 80 лет с нормальными показателями крови, моноклональный B-лимфоцитоз с иммунофенотипом ХЛЛ обнаруживается у 5 % людей в этой возрастной группе. Такой лимфоцитоз может прогрессировать в ХЛЛ со скоростью около 1 % в год[15].
Цитогенетическое исследование
[править | править код]Цитогенетическое исследование проводится методом стандартного кариотипирования или FISH. Задача исследования — выявление хромосомных мутаций, часть из которых имеет прогностическую значимость. Из-за возможности клональной эволюции исследование должно повторяться перед каждой линией терапии и в случае возникновения рефрактерности.
Стандартное кариотипирование возможно только для клеток в метафазе клеточного цикла. Так как злокачественные клетки при ХЛЛ обладают низкой митотической активностью, для получения необходимого для анализа количества метафаз требуется применение митогенов. Но даже в таком случае хромосомные мутации удаётся обнаружить только в 40—50 % случаев[16].
Интерфазная FISH при хроническом лимфоцитарном лейкозе не требует применения митогенов и отличается большей чувствительностью. При анализе используют локус-специфичные зонды, позволяющие выявлять наиболее распространённые хромосомные перестройки (как правило делеции). Этот метод позволяет детектировать хромосомные мутации в более чем 80 % случаев хронического лимфоцитарного лейкоза[16].
У каждого отдельного пациента может быть обнаружена одна, две и более стандартных мутации. Исследование, проведённое на 325 пациентах с хроническим лимфоцитарным лейкозом, позволило установить иерархию кариопитов по их прогностической способности: del17p, del11q, трисомия 12, нормальный кариотип и del13q. Если у пациента обнаружено больше одной мутации, то прогноз делают по той из них, которая находится выше в этом списке[16].

Хромосомные перестройки ассоциированы с определёнными клиническими характеристиками заболевания[16]:
- del13q14 выявляется в ~55 % случаев, делеция может быть моно- и биаллельной, заболевание, как правило, диагностируется на ранней стадии и развивается медленно, прогноз благоприятный;
- трисомия по хромосоме 12 выявляется в ~15 % случаев, прогноз обычный;
- del11q выявляется в ~15 % случаев, болезнь диагностируют на более поздних стадиях, выше вероятность проявления конституциональных симптомов, болезнь быстро прогрессирует, прогноз неблагоприятный, данная мутация может ассоциироваться с резистентностью к алкилирующим химиопрепаратам;
- del17p13 выявляется в ~7 % случаев, болезнь диагностируют на более поздних стадиях, выше вероятность проявления конституциональных симптомов, болезнь быстро прогрессирует, прогноз наиболее неблагоприятный, клоны часто бывают устойчивы к стандартным схемам химиотерапии с использованием алкилирующих препаратов и/или аналогов пурина[14];
- del6q21 характеризуется неблагоприятным прогнозом[3].
Другие методы
[править | править код]Рутинный физикальный осмотр позволяет получить достаточное представление о клинической динамике, поскольку заболевание носит системный характер. Выполнение УЗИ и компьютерной томографии для оценки объёма внутренних лимфоузлов не является обязательным вне клинических исследований.
Тест на гемолитическую анемию из-за высокой частоты аутоиммунных осложнений при ХЛЛ необходим даже при отсутствии её явных клинических проявлений. Рекомендуется проводить прямую пробу Кумбса, подсчёт числа ретикулоцитов и определение уровня фракций билирубина.
Как правило проведение биопсии костного мозга не требуется для поставки диагноза. Анализ биоптата может помочь сделать прогноз относительно скорости развития болезни, но последние наблюдения показывают, что использование других прогностических маркеров может давать лучшие результаты. Однако анализ аспирата или пунктата костного мозга может понадобиться для выяснения причин цитопении (специфическое поражение костного мозга или аутоиммунное осложнение) путём исследования миелограммы[14].
Некоторые дополнительные тесты используются для предсказания скорости прогрессирования заболевания, но не влияют на выбор схемы лечения. К таким тестам относится определение наличия соматических мутаций в вариабельной области генов тяжёлых цепей иммуноглобулинов (IgVH) и определение количества CD38 и ZAP-70 в клетках, поражённых хроническим лимфоцитарным лейкозом. IgVH без мутаций указывают для более агрессивную болезнь и менее благоприятный прогноз[17][18][19]. Экспрессия CD38 и ZAP-70 коррелирует с отсутствием мутаций в IgVH и плохим прогнозом. Однако пока не до конца ясно, являются ли эти молекулы независимыми прогностическими факторами[14]. Также на агрессивность болезни указывают повышенное количество тимидинкиназы[20], CD23[21] и β2-микроглобулина[22] в сыворотке крови.
Стадирование
[править | править код]Используются системы стадирования, предложенные K. Rai[23] и J. Binet[24]. Оригинальная система Rai была модифицирована с целью снизить количество определяемых групп риска с 5 до 3[14]. Обе системы опираются на данные физического осмотра и стандартные лабораторные анализы и легки в применении. В них отражено естественное течение заболевания — постепенное накопление опухолевой массы. Стадирование позволяет делать прогнозы о выживаемости: прогноз пациентов на поздних стадиях может быть хуже, чем на более ранних. Однако эти системы не дают возможности прогнозировать индивидуальный риск прогрессирования заболевания и выживания на ранних стадиях (стадии 0-II по Rai, A по Binet)[16]. По этой причине стали широко использовать другие прогностические маркеры, такие как цитогенетические характеристики злокачественных клонов, мутационный статус локуса IgVH и количество ZAP-70 или CD38.
|
| |||||||||||||||||||||||
Лечение
[править | править код]Хронический лимфолейкоз является практически неизлечимым медленнопрогрессирующим (индолентным) заболеванием.
Лечение не начинается сразу после подтверждения диагноза. Заболевание может сохранять стабильность годами, иногда в течение всей жизни больного. Часто наблюдается волнообразное течение с периодами увеличения и уменьшения опухолевого объема. Решение о необходимости начала терапии принимается обычно после периода более или менее длительного наблюдения.
Показания для начала лечения сформулированы в современных рекомендациях. Они отражают картину активной прогрессии заболевания, приводящей к ухудшению медицинского состояния больного и/или качества его жизни.
Из-за системного характера заболевания радиотерапия при хроническом лимфоцитарном лейкозе не применяется. Стандартом терапии являются химиотерапевтические режимы с включением нуклеотидных аналогов, алкилирующих препаратов и моноклональных антител.
Один из наиболее эффективных режимов — «FCR» (англ. fludarabine, cyclophosphamide, rituximab). Он позволяет получить полную ремиссию примерно у 85 % больных низкой группы риска. Однако этот режим имеет побочные эффекты, которые не позволяют использовать его для пациентов пожилого возраста. Кроме того, режим малоэффективен для больных группы высокого риска (например, имеющих делецию 17p)[25].
| Режим FCR | |
|---|---|
| Флударабин | 25 мг/м2 в/в или 40 мг/м2 р.о. 1—3 дни |
| Циклофосфамид | 250 мг/м2 в/в 1—3 дни |
| Ритуксимаб | 375 мг/м2 (1 курс) или 500 мг/м2 (2—6 курсы) 1 или 0 день |
Активно исследуется возможность применения в терапии алкилирующего препарата бендамустин.
Резистентость к цитостатикам, как правило, обусловлена нарушением механизмов инициации апоптоза в ответ на повреждения ДНК в клетках опухоли. Наиболее типичны мутации гена TP53, приводящие к его инактивации. Клетки с инактивированным p53 не погибают при накоплении повреждений генома. Более того, мутации, индуцированные цитостатиками, могут давать таким клеткам дополнительное преимущество за счет активации онкогенов или инактивации антионкогенов. Таким образом, мутагенез, индуцированный цитостатиками, может являться двигателем клональной эволюции.
У пациентов с резистентным течением в настоящее время используются высокие дозы глюкокортикостероидов, алемтузумаб (моноклональное антитело к CD52[26]), режимы, его содержащие, а также аллогенная трансплантация костного мозга.
Проведение интенсивной химиотерапии и трансплантации костного мозга у пожилых может быть затруднено плохим соматическим статусом и наличием серьезных сопутствующих заболеваний. В этой группе больных часто используется хлорамбуцил или комбинации на его основе.
Новые препараты (леналидомид, BGB-3111, акалабрутиниб, дувелисиб, умбралисиб) и комбинированные режимы на их основе в настоящее время проходят заключительные этапы клинических испытаний.
Существует также значительное количество новых экспериментальных подходов к терапии хронического лимфоцитарного лейкоза, эффективность и безопасность которых окончательно не установлена.
Таргетные препараты
[править | править код]В последние годы показана высокая эффективность ингибиторов тирозинкиназ Btk[27][28] (ибрутиниб, акалабрутиниб и др.) и PI3Kdelta (иделалисиб и др.), а также высокоселективного ингибитора Bcl-2 (венетоклакс). В 2014 году FDA (Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США) выдало разрешение на применение ибрутиниба у больных ХЛЛ, предварительно прошедших как минимум один курс лечения[29]. Данные таргетные препараты обладают высокой активностью даже у пациентов с неблагоприятным прогнозом (del17p) и относительно малотоксичны. В то же время, недостатком является их крайне высокая стоимость.
Моноклональные антитела: офатумумаб, обинутузумаб, моксетумомаб пасудотокс.
Прогноз
[править | править код]По клиническим проявлениям хронический лимфоцитарный лейкоз является довольно гетерогенным заболеванием: болезнь может протекать длительно без прогрессии или, наоборот, очень агрессивно[7]. Примерно в 30 % случаев болезнь прогрессирует медленно, так что смерть наступает по причине, не связанной с болезнью. В 15 % случаев смерть от болезни и/или побочных эффектов лечения наступает в течение 2—3 лет с момента постановки диагноза. В остальных случаях болезнь медленно прогрессирует в течение 5—10 лет, после чего наступает терминальная стадия заболевания, за которой следует смерть[30]. В случае пациентов из группы низкого риска медиана выживаемости от момента постановки диагноза достигает 8—10 лет. Известен ряд факторов, которые позволяют прогнозировать результаты лечения и продолжительность жизни, в том числе:
- Наличие или отсутствие признаков соматической гипермутации в генах вариабельных фрагментов иммуноглобулинов В-клеточного рецептора,
- Использование определенных V-генов в структуре В-клеточного рецептора (например, VH3—21),
- Уровень экспрессии тирозинкиназы Zap-70,
- Уровень экспрессии поверхностного маркера CD38,
- Хромосомные мутации del17p, del11q, затрагивающие гены TP53 и ATM,
- Уровень бета-2-микроглобулина в сыворотке крови,
- Стадия заболевания по Rai и Binet,
- Время удвоения числа лимфоцитов периферической крови и т. д.
Опухолевая трансформация, при которой клетки клона приобретают новые характеристики, делающие их похожими на диффузную крупноклеточную лимфому, носит название синдром Рихтера. Прогноз при наличии трансформации крайне неблагоприятный.
См. также
[править | править код]Примечания
[править | править код]- ↑ Disease Ontology (англ.) — 2016.
- ↑ Monarch Disease Ontology release 2018-06-29 — 2018-06-29 — 2018.
- ↑ 1 2 3 4 Chiorazzi N., Rai K. R., Ferrarini M. Chronic lymphocytic leukemia // N Engl J Med. — 2005. — Т. 352, вып. 8. — С. 804—815. — PMID 15728813.
- ↑ Jemal A., Siegel R., Xu J., Ward E. Cancer statistics, 2010 // CA Cancer J Clin. — 2010. — Т. 60, вып. 5. — С. 277—300. — doi:10.3322/caac.20073. — PMID 20610543. Архивировано 11 июня 2012 года.
- ↑ 1 2 3 Kipps T. J., Stevenson F. K., Wu C. J., Croce C. M., Packham G., Wierda W. G., O'Brien S., Gribben J., Rai K. Chronic lymphocytic leukaemia. (англ.) // Nature reviews. Disease primers. — 2017. — Vol. 3. — P. 16096. — doi:10.1038/nrdp.2016.96. — PMID 28102226.
- ↑ Cerhan J. R., Slager S. L. Familial predisposition and genetic risk factors for lymphoma. (англ.) // Blood. — 2015. — Vol. 126, no. 20. — P. 2265—2273. — doi:10.1182/blood-2015-04-537498. — PMID 26405224.
- ↑ 1 2 3 Gaidano G., Foà R., Dalla-Favera R. Molecular pathogenesis of chronic lymphocytic leukemia // J Clin Invest. — 2012. — Т. 122, вып. 10. — С. 3432-3438. — doi:10.1172/JCI64101. — PMID 23023714.
- ↑ Baumann Kreuziger L. M., Tarchand G., Morrison V. A. The impact of Agent Orange exposure on presentation and prognosis of patients with chronic lymphocytic leukemia. (англ.) // Leukemia & lymphoma. — 2014. — Vol. 55, no. 1. — P. 63—66. — doi:10.3109/10428194.2013.794267. — PMID 23573826.
- ↑ Schinasi L. H., De Roos A. J., Ray R. M., Edlefsen K. L., Parks C. G., Howard B. V., Meliker J. R., Bonner M. R., Wallace R. B., LaCroix A. Z. Insecticide exposure and farm history in relation to risk of lymphomas and leukemias in the Women's Health Initiative observational study cohort. (англ.) // Annals of epidemiology. — 2015. — Vol. 25, no. 11. — P. 803—810. — doi:10.1016/j.annepidem.2015.08.002. — PMID 26365305.
- ↑ Dameshek W. Chronic lymphocytic leukemia — an accumulative disease of immunologically incompetent lymphocytes // Blood. — 1967. — Т. 29, вып. 4:Suppl. — С. 566—584. — PMID 6022294.
- ↑ Messmer B. T., Messmer D., Allen S. L., Kolitz J. E., Kudalkar P., Cesar D., Murphy E. J., Koduru P., Ferrarini M., Zupo S., Cutrona G., Damle R. N., Wasil T., Rai K. R., Hellerstein M. K., Chiorazzi N. In vivo measurements document the dynamic cellular kinetics of chronic lymphocytic leukemia B cells // J Clin Invest. — 2005. — Т. 115, вып. 3. — С. 755—764. — doi:10.1172/jci23409.
- ↑ D'Cruz O. J., Uckun F. M. Novel Bruton's tyrosine kinase inhibitors currently in development // Onco Targets Ther. — 2013. — Т. 6. — С. 161—176. — doi:10.2147/OTT.S33732. — PMID 23493945. Архивировано 15 июня 2022 года.
- ↑ Krysov S., Dias S., Paterson A., Mockridge C. I., Potter K. N., Smith K. A., Ashton-Key M., Stevenson F. K., Packham G. Surface IgM stimulation induces MEK1/2-dependent MYC expression in chronic lymphocytic leukemia cells. (англ.) // Blood. — 2012. — Vol. 119, no. 1. — P. 170—179. — doi:10.1182/blood-2011-07-370403. — PMID 22086413.
- ↑ 1 2 3 4 5 6 7 8 Hallek M., Cheson B. D., Catovsky D. et al. Guidelines for the diagnosis and treatment of chronic lymphocytic leukemia: a report from the International Workshop on Chronic Lymphocytic Leukemia updating the National Cancer Institute-Working Group 1996 guidelines // Blood. — 2008. — Т. 111, вып. 12. — С. 5446-5456. — doi:10.1182/blood-2007-06-093906. — PMID 18216293. Архивировано 25 мая 2021 года.
- ↑ 1 2 3 Rawstron A. C., Bennett F. L., O'Connor S. J., Kwok M., Fenton J. A., Plummer M., de Tute R., Owen R. G., Richards S. J., Jack A. S., Hillmen P. Monoclonal B-cell lymphocytosis and chronic lymphocytic leukemia // N Engl J Med. — 2008. — Вып. 359, № 6. — С. 575-83. — doi:10.1056/NEJMoa075290. — PMID 18687638. Архивировано 21 июля 2014 года.
- ↑ 1 2 3 4 5 Döhner H., Stilgenbauer S., Benner A., Leupolt E., Kröber A., Bullinger L., Döhner K., Bentz M., Lichter P. Genomic aberrations and survival in chronic lymphocytic leukemia // N Engl J Med. — 2000. — Т. 343, № 26. — С. 1910-6. — PMID 11136261. Архивировано 15 февраля 2015 года.
- ↑ Damle R. N., Wasil T., Fais F., Ghiotto F., Valetto A., Allen S. L., Buchbinder A., Budman D., Dittmar K., Kolitz J., Lichtman S. M., Schulman P., Vinciguerra V. P., Rai K. R., Ferrarini M., Chiorazzi N. Ig V gene mutation status and CD38 expression as novel prognostic indicators in chronic lymphocytic leukemia. (англ.) // Blood. — 1999. — Vol. 94, no. 6. — P. 1840—1847. — PMID 10477712.
- ↑ Hamblin T. J., Davis Z., Gardiner A., Oscier D. G., Stevenson F. K. Unmutated Ig V(H) genes are associated with a more aggressive form of chronic lymphocytic leukemia. (англ.) // Blood. — 1999. — Vol. 94, no. 6. — P. 1848—1854. — PMID 10477713.
- ↑ Hamblin T. J., Orchard J. A., Ibbotson R. E., Davis Z., Thomas P. W., Stevenson F. K., Oscier D. G. CD38 expression and immunoglobulin variable region mutations are independent prognostic variables in chronic lymphocytic leukemia, but CD38 expression may vary during the course of the disease. (англ.) // Blood. — 2002. — Vol. 99, no. 3. — P. 1023—1029. — PMID 11807008.
- ↑ Hallek M., Langenmayer I., Nerl C., Knauf W., Dietzfelbinger H., Adorf D., Ostwald M., Busch R., Kuhn-Hallek I., Thiel E., Emmerich B. Elevated serum thymidine kinase levels identify a subgroup at high risk of disease progression in early, nonsmoldering chronic lymphocytic leukemia. (англ.) // Blood. — 1999. — Vol. 93, no. 5. — P. 1732—1737. — PMID 10029603.
- ↑ Knauf W. U., Langenmayer I., Ehlers B., Mohr B., Adorf D., Nerl C. H., Hallek M., Zwingers T. H., Emmerich B., Thiel E. Serum levels of soluble CD23, but not soluble CD25, predict disease progression in early stage B-cell chronic lymphocytic leukemia. (англ.) // Leukemia & lymphoma. — 1997. — Vol. 27, no. 5-6. — P. 523—532. — doi:10.3109/10428199709058320. — PMID 9477135.
- ↑ Gentile M., Cutrona G., Neri A., Molica S., Ferrarini M., Morabito F. Predictive value of beta2-microglobulin (beta2-m) levels in chronic lymphocytic leukemia since Binet A stages. (англ.) // Haematologica. — 2009. — Vol. 94, no. 6. — P. 887—888. — doi:10.3324/haematol.2009.005561. — PMID 19483161.
- ↑ Rai K. R., Sawitsky A., Cronkite E. P., Chanana A. D., Levy R. N., Pasternack B. S. Clinical staging of chronic lymphocytic leukemia // Blood. — 1975. — Т. 46, вып. 2. — С. 219—234. — PMID 1139039. Архивировано 21 февраля 2013 года.
- ↑ Binet J. L., Auquier A., Dighiero G., Chastang C., Piguet H., Goasguen J., Vaugier G., Potron G., Colona P., Oberling F., Thomas M., Tchernia G., Jacquillat C., Boivin P., Lesty C., Duault M. T., Monconduit M., Belabbes S., Gremy F. A new prognostic classification of chronic lymphocytic leukemia derived from a multivariate survival analysis // Cancer. — 1981. — Т. 48, вып. 1. — С. 198-206. — PMID 7237385.
- ↑ Riches J. C., Ramsay A. G., Gribben J. G. Chronic lymphocytic leukemia: an update on biology and treatment // Curr Oncol Rep. — 2011. — Т. 13, вып. 5. — С. 379-385. — doi:10.1007/s11912-011-0188-6. — PMID 21773694.
- ↑ Лекарство, применяемое при лейкемии, может стать мощным оружием в борьбе против рассеянного склероза. Дата обращения: 23 октября 2008. Архивировано 26 октября 2008 года.
- ↑ O'Brien S., Furman R. R., Coutre S. E., Sharman J. P., Burger J. A., Blum K. A., Grant B., Richards D. A., Coleman M., Wierda W. G., Jones J. A., Zhao W., Heerema N. A., Johnson A. J., Izumi R., Hamdy A., Chang B. Y., Graef T., Clow F., Buggy J. J., James D. F., Byrd J. C. Ibrutinib as initial therapy for elderly patients with chronic lymphocytic leukaemia or small lymphocytic lymphoma: an open-label, multicentre, phase 1b/2 trial. (англ.) // The lancet oncology. — 2014. — Vol. 15, no. 1. — P. 48—58. — doi:10.1016/S1470-2045(13)70513-8. — PMID 24332241.
- ↑ Byrd J. C., Furman R. R., Coutre S. E., Flinn I. W., Burger J. A., Blum K. A., Grant B., Sharman J. P., Coleman M., Wierda W. G., Jones J. A., Zhao W., Heerema N. A., Johnson A. J., Sukbuntherng J., Chang B. Y., Clow F., Hedrick E., Buggy J. J., James D. F., O'Brien S. Targeting BTK with ibrutinib in relapsed chronic lymphocytic leukemia. (англ.) // The New England journal of medicine. — 2013. — Vol. 369, no. 1. — P. 32—42. — doi:10.1056/NEJMoa1215637. — PMID 23782158.
- ↑ FDA NEWS RELEASE. Дата обращения: 24 июля 2014. Архивировано 15 декабря 2014 года.
- ↑ Spaargaren M., de Rooij M. F., Kater A. P., Eldering E. BTK inhibitors in chronic lymphocytic leukemia: a glimpse to the future. (англ.) // Oncogene. — 2015. — Vol. 34, no. 19. — P. 2426—2436. — doi:10.1038/onc.2014.181. — PMID 24954503.
Ссылки
[править | править код]- Патологическая анатомия. Курс лекций. Под ред. В. В. Серова, М. А. Пальцева. — М.: Медицина, 1998